« Berkélium » : différence entre les versions
Contenu supprimé Contenu ajouté
Isotopes |
→Historique : image déplacée dans l'infobox |
||
| Ligne 3 : | Ligne 3 : | ||
== Historique == |
== Historique == |
||
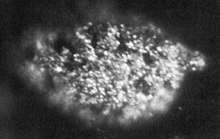
[[Image:Berkelium metal.jpg|vignette|[[Microphotographie]] d'un échantillon de berkélium pur.|left]] |
|||
Il a été synthétisé pour la première fois en décembre [[1949]] par [[Stanley G. Thompson]], [[Glenn Theodore Seaborg]], [[Kenneth Street, Jr.]], et [[Albert Ghiorso]] à l'[[université de Californie à Berkeley]]. Le premier [[isotope]] produit a un nombre de masse de 243 et se dégrade avec une [[demi-vie]] de 4,5 heures. Dix autres isotopes ont été synthétisés depuis. En raison de sa rareté, le berkélium n'a actuellement aucune utilisation commerciale. |
Il a été synthétisé pour la première fois en décembre [[1949]] par [[Stanley G. Thompson]], [[Glenn Theodore Seaborg]], [[Kenneth Street, Jr.]], et [[Albert Ghiorso]] à l'[[université de Californie à Berkeley]]. Le premier [[isotope]] produit a un nombre de masse de 243 et se dégrade avec une [[demi-vie]] de 4,5 heures. Dix autres isotopes ont été synthétisés depuis. En raison de sa rareté, le berkélium n'a actuellement aucune utilisation commerciale. |
||
Version du 11 juillet 2016 à 11:02
Le berkélium est un élément chimique transuranien de symbole Bk et de numéro atomique 97.
Historique
Il a été synthétisé pour la première fois en décembre 1949 par Stanley G. Thompson, Glenn Theodore Seaborg, Kenneth Street, Jr., et Albert Ghiorso à l'université de Californie à Berkeley. Le premier isotope produit a un nombre de masse de 243 et se dégrade avec une demi-vie de 4,5 heures. Dix autres isotopes ont été synthétisés depuis. En raison de sa rareté, le berkélium n'a actuellement aucune utilisation commerciale.
Composés
Isotopes
20 radioisotopes sont connus, de 235Bk à 254Bk et 6 isomères nucléairess. L'isotope a la plus grande demi-vie est 247Bk avec une demi-vie de 1 380 ans.
Notes et références
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, , 89e éd., p. 10-203
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, , 90e éd., 2804 p., Relié (ISBN 978-1-420-09084-0)
- Base de données Chemical Abstracts interrogée via SciFinder Web le 15 décembre 2009 (résultats de la recherche)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| 8 | 119 | 120 | * | ||||||||||||||||||||||||||||||
| * | 121 | 122 | 123 | 124 | 125 | 126 | 127 | 128 | 129 | 130 | 131 | 132 | 133 | 134 | 135 | 136 | 137 | 138 | 139 | 140 | 141 | 142 | |||||||||||
| Métaux Alcalins |
Alcalino- terreux |
Lanthanides | Métaux de transition |
Métaux pauvres |
Métal- loïdes |
Non- métaux |
Halo- gènes |
Gaz nobles |
Éléments non classés |
| Actinides | |||||||||
| Superactinides | |||||||||